« Anode » et « cathode » sont des termes fondamentaux utilisés dans l’électrochimie et les circuits électroniques. Ces deux types d’électrodes jouent un rôle important dans une variété de systèmes, des batteries simples aux technologies avancées.
Examinons leurs différences, leurs étiquettes positives et négatives, et comment savoir facilement laquelle est négative ou positive.
Table des matières
Qu’est-ce qu’une électrode ?
Il est important que vous compreniez l’idée générale de ce qu’est vraiment une électrode avant d’entrer dans les subtilités de ce qu’est une cathode ou une anode. Au sens le plus élémentaire, une électrode est un matériau qui facilite la conduction de l’électricité, permettant au courant électrique d’entrer ou de sortir d’un milieu non métallique, tel qu’une cellule électrolytique.
En termes simples, une électrode sert de conducteur pour établir un contact électrique avec un composant non métallique du circuit.
Qu’est-ce qu’une anode ?

La polarité d’une électrode, qu’il s’agisse d’une anode ou d’une cathode, dépend du type de circuit. L’anode est l’électrode où se produit l’oxydation, entraînant la perte d’électrons. En regardant ce qui se passe dans une cellule galvanique (qui convertit l’énergie chimique en électricité, comme une décharge de batterie), l’anode agit comme l’électrode négative puisque, pendant l’oxydation, les électrons sont laissés sur l’électrode et circulent à travers le circuit externe.
Inversement, dans l’électrolyse, où un courant électrique entraîne le flux d’électrons dans la direction opposée, l’anode devient l’électrode positive.
Qu’est-ce qu’une cathode ?
 Crédit d’image : Tarte aux framboises
Crédit d’image : Tarte aux framboises
La cathode sert de site où se produit la réduction, facilitant le gain d’électrons. Dans une cellule galvanique, il agit comme l’électrode positive puisque les ions subissent une réduction en acquérant des électrons de l’électrode et ensuite se plaquent.
D’autre part, dans l’électrolyse, la cathode est la borne négative, attirant les ions positifs de la solution.
Anode contre cathode : clarifier la polarité
Au départ, on croyait que l’électricité circulait du positif au négatif, à l’opposé de ce que nous comprenons maintenant comme étant vrai. Cette idée fausse précoce a conduit certains à associer l’anode à la négativité et la cathode à la positivité.
Cependant, avec une bonne compréhension des rôles de l’oxydation et de la réduction dans chaque électrode, il devient facile d’identifier laquelle est l’anode ou la cathode, cela dépend du type de circuit.
Qu’est-ce qu’un électrolyte dans une batterie ?
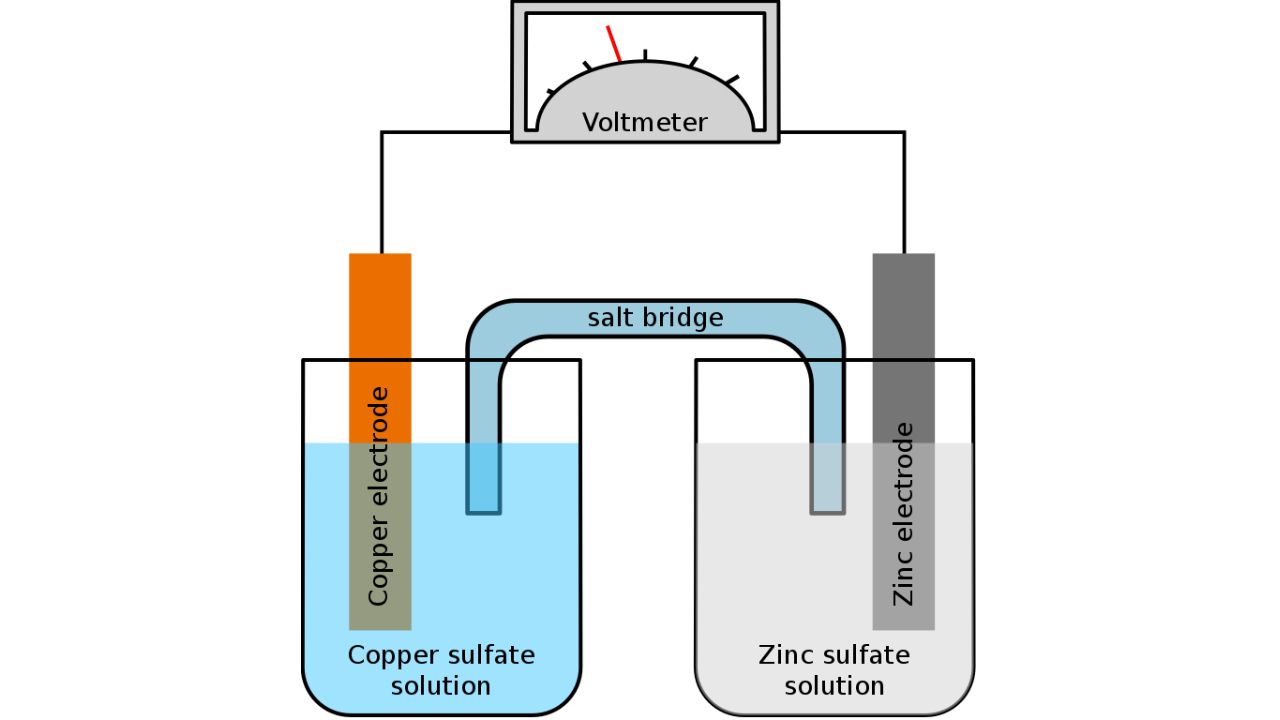 Crédit image : Tinux/gringer/Wikimédia Commons
Crédit image : Tinux/gringer/Wikimédia Commons
Dans les batteries, l’électrolyte fait référence au milieu qui permet la circulation des ions entre l’anode et la cathode tout en les gardant électriquement neutres. Ce mouvement ionique est essentiel pour les réactions chimiques qui se produisent lors des processus de charge et de décharge. Pour en savoir plus à ce sujet, lisez comment fonctionnent les batteries lithium-ion pour véhicules électriques.
Lequel est positif ?
Pour comprendre les polarités lorsque l’on parle d’électrodes dans une cellule ou un circuit, il est important de considérer les deux réactions qui se produisent sur les deux sites. Dans une cellule galvanique, l’anode subit une oxydation et fonctionne comme l’électrode négative, tandis que dans l’électrolyse, elle devient l’électrode positive. Inversement, la cathode facilite la réduction et sert d’électrode positive dans une cellule galvanique mais agit comme borne négative dans l’électrolyse.

